去年曾经“摇摇欲坠”的TIGIT靶点,如今又一次走到聚光灯下,而这一次,很有可能重新点燃细分领域的创新激情。
近日,ASCO官网发布信息,罗氏披露了TIGIT单抗Tiragolumab联合疗法一线治疗不可切除的局部晚期或转移性肝细胞癌(uHCC)患者的早期数据。

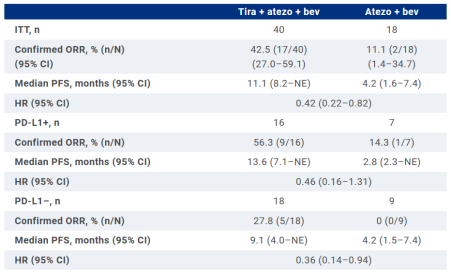
在此之前,罗氏“T+A”疗法已经成为肝癌治疗的一线标准疗法,此次公布的临床数据发现,在加上TIGIT抗体tiragolumab 之后,ORR从11.1%提高到42.5%,mPFS从4.2个月提高到11.1个月,均提高到3倍左右,疾病进展或死亡风险降低58%。有望为 uHCC 患者提供新的一线治疗方案,并支持进一步的临床研究。
此次公布的临床数据,为历经临床挫折的TIGIT靶点带来了新的希望。事实上,TIGIT成药之路,举步维艰。
在过去的一年时间里,默沙东、罗氏等企业在PD-1/L1+TIGIT联合疗法的连续受挫,近期BMS公布2022年财报之际,同时宣布由于安全性问题,决定终止TIGIT抑制剂BMS-986207的II期临床试验。无疑给TIGIT这个曾经快速蹿红的潜力靶点再次蒙上一层阴霾。
然而,医药创新本身就是一个科学探索的过程,我们既不能盲目乐观,也不需要过度悲观。TIGIT抑制剂充满未知的前景,并未打消先行者和后来者的决心,在 2023 年度 ASCO 年会上,除了罗氏,还有默沙东、吉利德、百济神州这三位第一梯队企业公布新数据;同时也有新秀露面,阿斯利康、泽璟制药的双抗均为首次亮相。
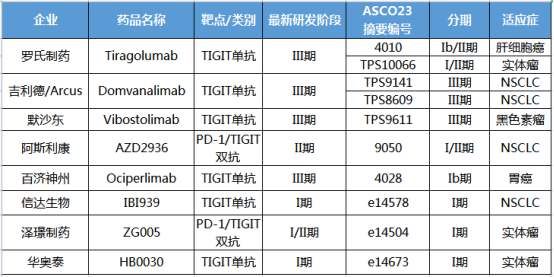
2023 ASCO - TIGIT 靶点临床数据披露,仅为人工筛选,不代表全部数据
接连受挫后迎来曙光?
Tiragolumab 是进度最快的TIGIT单抗,其临床研究始于 2016 年度,已登记 48 项临床试验,其中包括 7 个 III 期临床。目前,罗氏正在非小细胞癌症(NSCLC)、小细胞肺癌(SCLC)和食管鳞状细胞癌(ESCC)中开展临床III期研究,评估Tiragolumab单药或联合疗法的疗效。
据了解,本届 ASCO 披露的是MORPHEUS-Liver 临床数据,MORPHEUS-Liver 是系列研究中针对肝细胞癌的一项试验,其中包含了联用 Tiragolumab 的队列;既往未经治疗的 uHCC 患者随机分配,分别接受阿替利珠单抗(1200mg IV)联用贝伐珠单抗(15mg/kg IV)加或不加 Tiragolumab(600mg IV)每 3 周一次治疗。试验主要终点为研究者根据 RECIST V1.1 评估的 ORR,次要终点包括 PFS 和安全性。
Ib/II期Morpheus-Liver研究显示,与对照组(阿替利珠单抗 + 贝伐珠单抗,n = 18)相比,TIGIT单抗Tiragolumab+阿替利珠单抗+贝伐珠单抗联合治疗组(n = 40)获得了更高的客观缓解率(ORR)和更长的无进展生存期(PFS)。
安全性方面,tiragolumab联合治疗组与对照组发生3/4级治疗相关不良反应的概率分别为27.5%和33.3%,发生导致任何治疗中止的不良反应的概率为22.5%和22.2%。
然而,就目前的临床探索进展而言,TIGIT能否走向成功还是一个未知数。2022年,罗氏作为TIGIT靶点进展最快的玩家,重重地栽了跟头。
2022年3月,由罗氏研发的TIGIT单抗Tiragolumab联合PD-L1单抗Tecentriq和化疗一线治疗广泛期小细胞肺癌(ES-SCLC)的III期临床SKYSCRAPER-02研究未能达到无进展生存期(PFS)和总生存期(OS)共同主要终点。这也是全球首个TIGIT三期临床的失败。
短短两个月后,2022年5月,罗氏公布其TIGIT单抗产品Tiragolumabb的第二个III期试验失败。TIGIT单抗Tiragolumab联合PD-L1单抗Tecentriq联用治疗PD-L1高表达局部晚期或转移性非小细胞肺癌(NSCLC)的Ⅲ期临床未能达到无进展生存期(PFS)主要终点,另一个主要终点总生存期(OS)尚未成熟。
巨头的连续失败,直接动摇了细分赛道参与者的信心。今年2月,百时美施贵宝决定终止TIGIT抑制剂BMS-986207的II期临床试验,该药是与CTLA-4抑制剂Yervoy、PD-1抑制剂Opdivo构成三联疗法的一部分。此前,因临床数据良好,行业对BMS-986207的期待值仅次于罗氏TIGIT抗体tiragolumab。即使在去年12月,BMS-986207与Opdivo、Compugen靶向PVRIG抗体COM701的组合疗法也在卵巢癌患者中取得积极结果,不禁令人唏嘘。
肿瘤免疫持续火爆
能否成为下一个PD-1?
PD-1作为最广为人知的免疫检查点,其靶向药物在临床上取得了巨大的成功,在多种肿瘤治疗中展现积极疗效。2022年,KEYTRUDA销售额达到209.37亿美元,同比增长22%,距离“药王”修美乐仅一步之遥,肿瘤免疫治疗已经毫无疑问成为了创新药市场的“顶流”。
在PD-1之后,人们致力于寻找到下一个有望成为重磅药物的免疫检查点抑制剂,作为免疫细胞上的一种蛋白质受体,TIGIT是具有潜力的免疫检查点之一。
和PD-1类似,TIGIT起到抑制免疫反应的作用,实体瘤细胞可以利用TIGIT来避免被免疫系统检测到。TIGIT单抗类药物通过与TIGIT结合,有望再次激活免疫反应,攻击和杀死靶细胞。
但作为最具有潜力的免疫检查点之一,TIGIT仍有不少门槛需要跨越。最明显的“硬伤”就是TIGIT单药疗效低,而联用效果似乎又不稳定。TIGIT单抗联合疗法接连受挫,并未影响TIGIT赛道的研发热潮。
根据公开数据显示,当前全球共有超过50个TIGIT抗体药项目在开发,其中多数个为单抗项目,进展最快的4个TIGIT单抗都已经处于III期临床,相应药企都投入了极大的资源在推进。
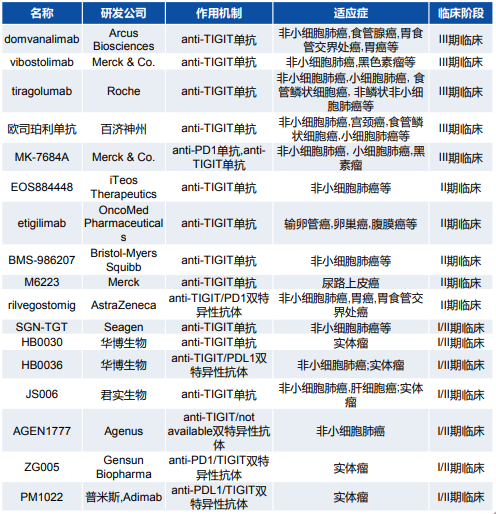
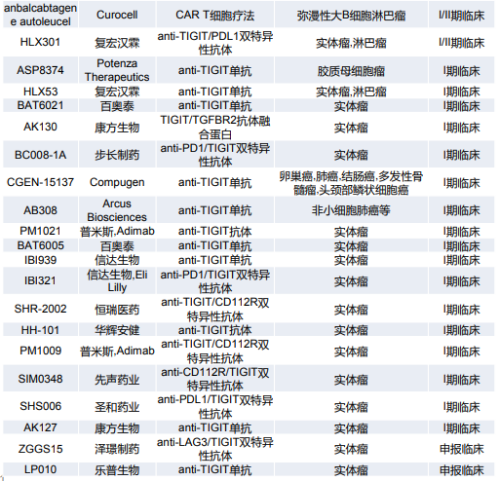
TIGIT靶向药物研发进度 信息来源:企业官网、华创研究
不只是BMS、罗氏、默沙东等MNC,国内企业同样是 TIGIT 靶点上的重度参与者。
公开数据显示,这一靶点的在研项目中,15个有中国企业的身影。甚至,百济神州仅次于罗氏,在第一梯队4家III期阶段项目中占据一席之地。
信达生物是第一家在国内开展TIGIT药物临床研究的企业。去年ESMO IO大会上,信达生物公布了TIGIT单抗IBI939联合信迪利单抗一线治疗非小细胞肺癌临床数据。当时,信达生物制药集团高级副总裁周辉表示,该研究展现出较长的无进展生存期,接受联合治疗的受试者发生的安全性事件整体可控,未出现新的安全性信号。
2021年10月,康方生物的TIGIT抑制剂AK127联合PD-1/CTLA-4双抗AK104治疗晚期或转移性实体瘤的I期临床试验,在澳大利亚完成首例患者给药。
非临床资料显示,AK127具有高效阻断TIGIT/PVR相互作用的生物活性。而PVR是TIGIT的生理性配体,两者结合会抑制T细胞及NK细胞活性。这提示,AK127可有效接触免疫细胞活性抑制,使免疫细胞恢复正常免疫功能。
除了上述本土药企之外,恒瑞医药、君实生物、步长制药、百奥泰等纷纷入局。
尽管此前已经有许多新兴靶点研发临床试验失败的案例,而TIGIT抗体药的研发也尚在摸索当中。此次罗氏PD-L1+VEGF+TIGIT再获积极数据,为TIGIT靶点带来了新的希望。这也说明了联合治疗临床探索的复杂性,同时为后续临床探索提供了重要的借鉴,期待“下一个PD-1”早日出现。
编辑:艾伦