实验虐你千百遍,改做生信你会收获意外的惊喜~实验赛道卷不过就换个赛道试试水吧!选择生信肯定会让你眼前一亮又一亮!想快速发文的你算是捞着了!思路简单让人很难不心动哇!
今天豆豆带来的这篇文章肯定对你胃口,模版现成,属实是生信小白友好型文章~这篇中国医科大团队的文章《Development and validation of a prognostic and drug sensitivity model for gastric cancer utilizing telomere-related genes》带你走进生信大世界~
1、本研究通过整合数据库中的转录组数据,筛选出多个与肿瘤预后显著相关的基因,从而构建风险模型,并进行外部验证,为疾病的精准预后评估提供了新的视角。在医学界,肿瘤是永不过时的研究疾病,目前肿瘤生信发文热度也是只增不减。常规思路也能纯生信发文,这个赛道也没想象的卷嘛,其实有时宝子们不需要太多花哨的分析+实验,常规做到极致就是好文章。
2、本研究通过比较组别之间免疫细胞浸润的差异,分析了不同风险组的肿瘤免疫微环境,明确了预后差异的潜在免疫学机制。
Ps:像这篇文章提到了肿瘤免疫微环境这一热点,我们在发文的时候如果能结合一些热点方向,比如细胞程序性死亡中的铁死亡、铜死亡或者最近新发现的钠死亡等,都是肿瘤方向研究的热点文章分值可能会上个台阶哦~想快速发文又愁没思路,对生信感兴趣想学习的宝子们可以找豆豆聊聊,豆豆随时恭候~

题目:利用端粒相关基因建立胃癌预后及药物敏感性模型并进行验证
杂志:Translational oncology
影响因子:IF=4.5
发表时间:2024年12月
研究背景
胃癌是全球第五大常见癌症,常导致晚期诊断,预后不良,5年生存率仅为10%-30%,是全球面临的重大健康挑战。在染色体稳定性中,端粒扮演者重要角色。在胃癌中,端粒酶活性的升高会导致肿瘤的快速生长和侵袭,因此研究端粒相关基因(TRGs)的表达模式可以提高对端粒相关胃癌进展机制的理解,并将其作为胃癌多种治疗策略的潜在靶点。
数据来源
Dataset |
Platform | Number of samples(groups) |
GSE62254 | GPL570 [HG-U133_Plus_2] Affymetrix Human Genome U133 Plus 2.0 Array | 300名GC患者样本的RNA-seq |
TCGA_SRTAD | UCSC Xena | 334名GC患者样本的RNA-seq |
研究思路
本研究以TCGA和GEO数据库的转录组数据为来源结合临床信息,获得多个差异表达基因并进行筛选,通过Cox单变量回归和LASSO-Cox回归分析构建了一个包含四个关键基因的预后风险模型,随后进行免疫细胞浸润分析,并结合药物敏感性分析探讨了基于风险分层的个体化治疗潜力。最终,结合临床特征构建列线图,为胃癌患者的精准预后评估和治疗选择提供了新的工具和理论依据。Ps:如果你还在为拿到手的数据发愁没有思路的话,就来找豆豆吧,关注豆豆不迷路!豆豆带你生信走花路!
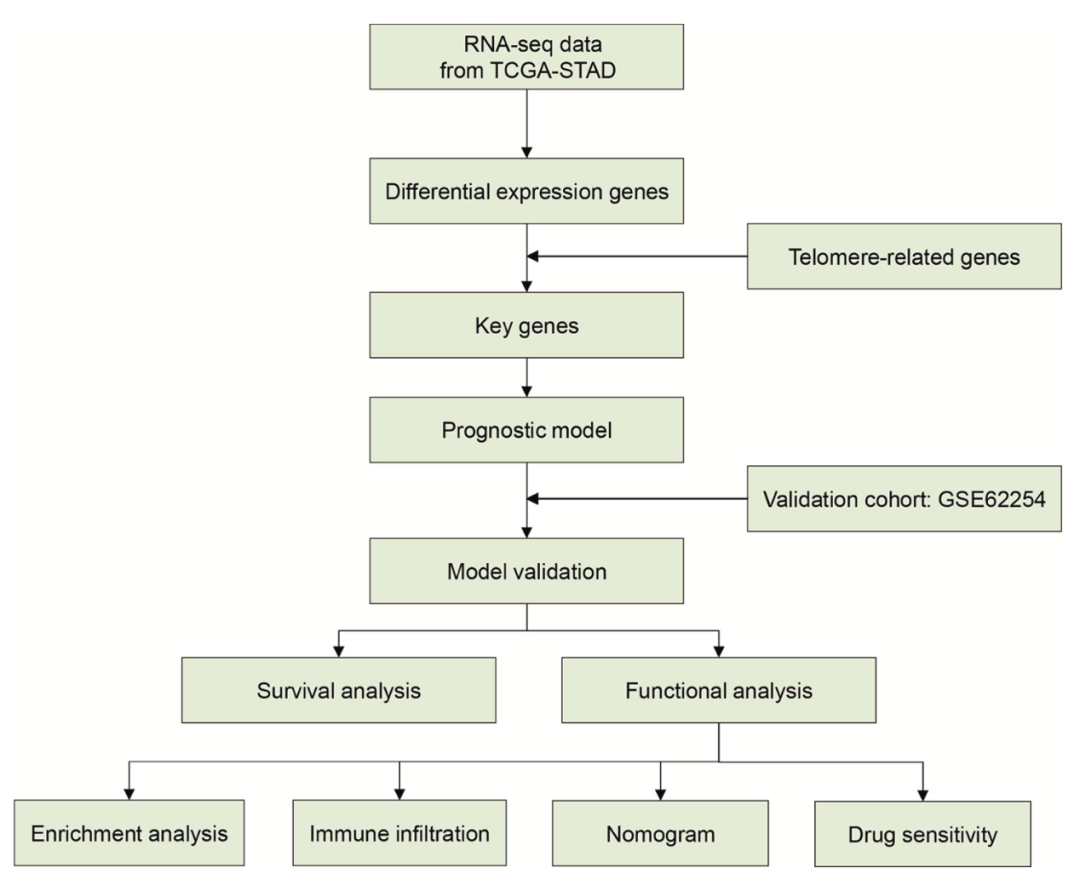
研究结果
差异表达分析
334名患者的肿瘤组织对照正常组织筛选差异基因,共鉴定出8939个DEG,其中5713个DEG被显著上调(图1A)。在TelNet数据库中筛选出2093个TRG,将这些TRG与上述筛选到的DEG进行比对,其中的328个DEG与TRG重叠(图1B)。
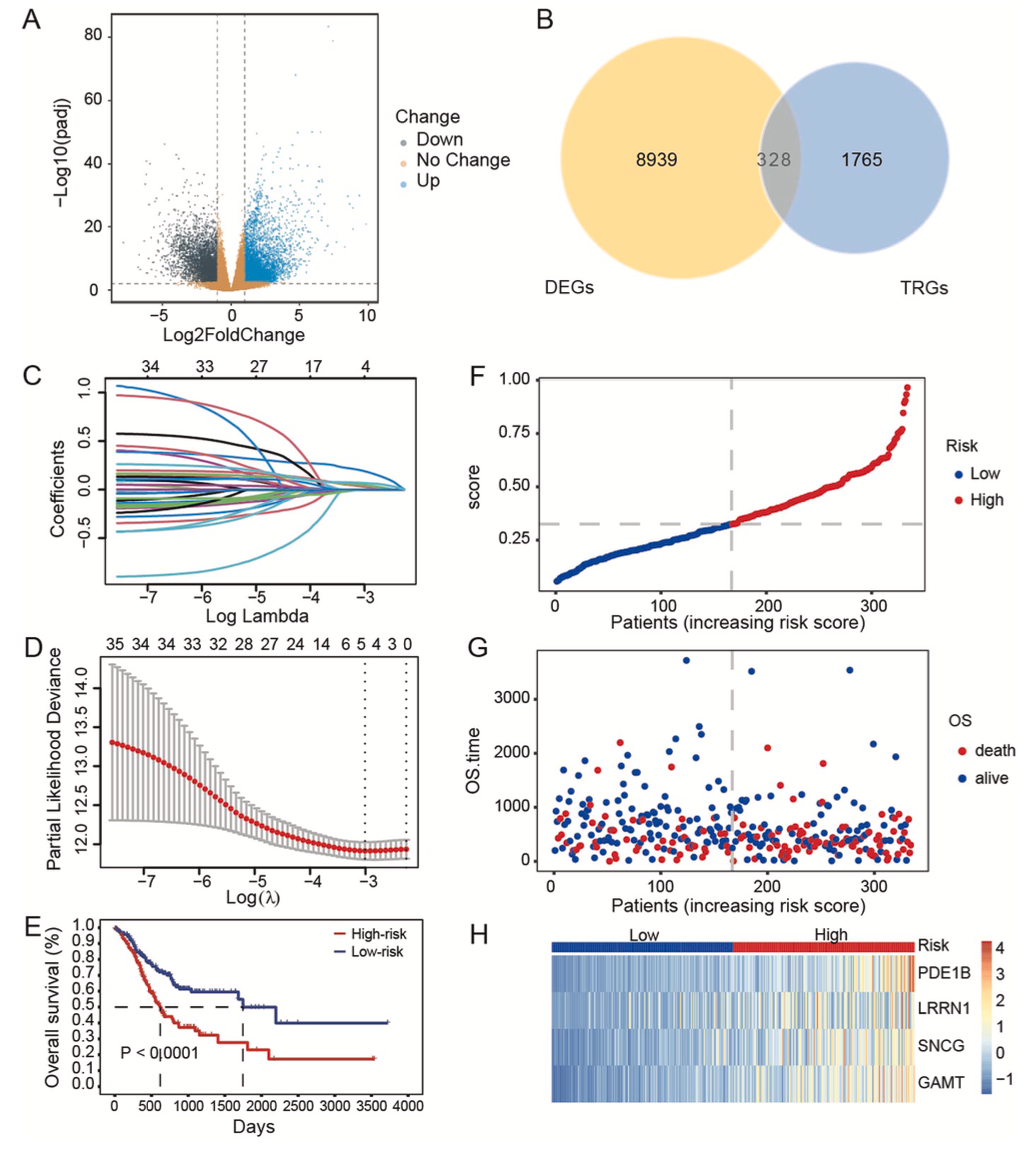
风险模型的构建
通过Cox单变量回归分析,确定了35个与OS显著相关的TRG,利用LASSO-Cox回归算法从35个关键TRG中选择了LRRN1、SNCG、GAMT和PDE1B作为模型基础构建预后风险模型(图1C,D)。KM分析显示,随着风险评分增加LRRN1、SNCG、GAMT和PDE1B表达水平也增加,存在有一定的正相关(图1E,F),高风险组的死亡率高于低风险组(图1G),在高风险组中,这四个关键TRG表达水平更高(图1H)。
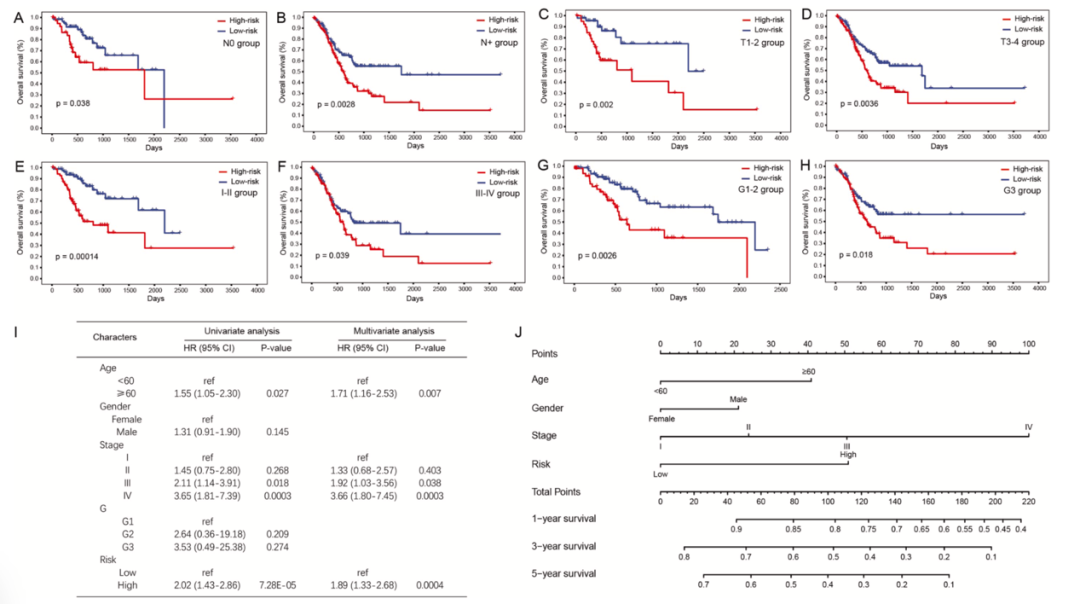
临床亚组分析及列线图模型构建
高风险组患者年龄小于60岁的比例更高,且淋巴结受累和肿瘤分化差的比例更高(图2A-H)。基于临床特征和风险评分的Cox回归分析显示,年龄大于或等于60岁、III期和IV期以及高风险评分是OS的独立预后因素(图2I)。然后以这几个独立预后因素为基础,以列线图的形式预测了1年、3年和5年的存活率(图2J),体现了预后模型的临床应用价值,从而为患者的治疗决策提供科学依据。
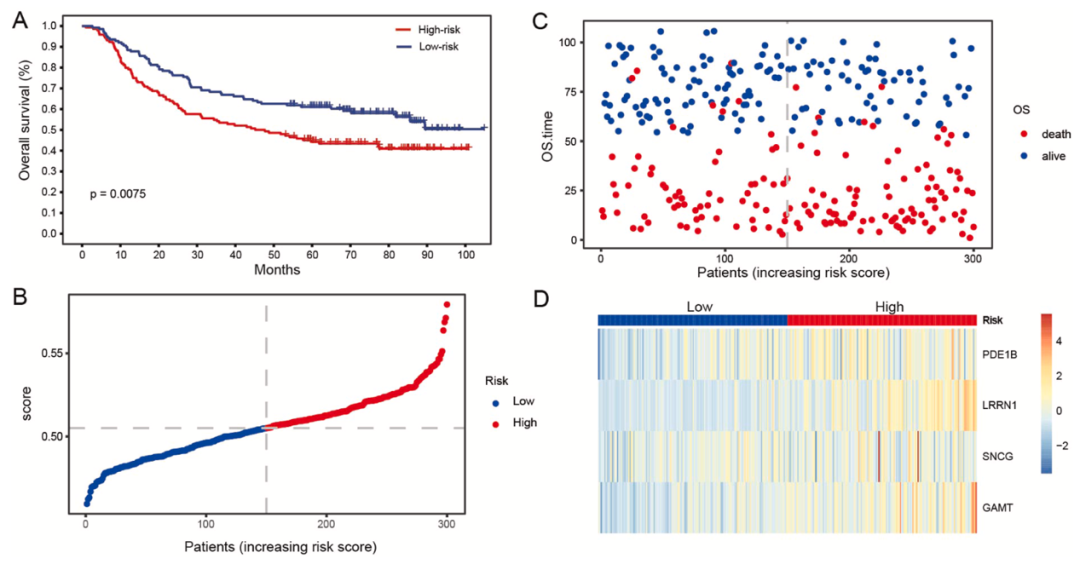
预后风险模型验证
使用GSE62254验证预后风险模型(图3A,B),其结果显示良好。风险评分越高(图3C)意味着LRRN1、SNCG、GAMT和
PDE1B表达水平越高(图3D)。这些结果证明了构建的预后风险模型的有效性。
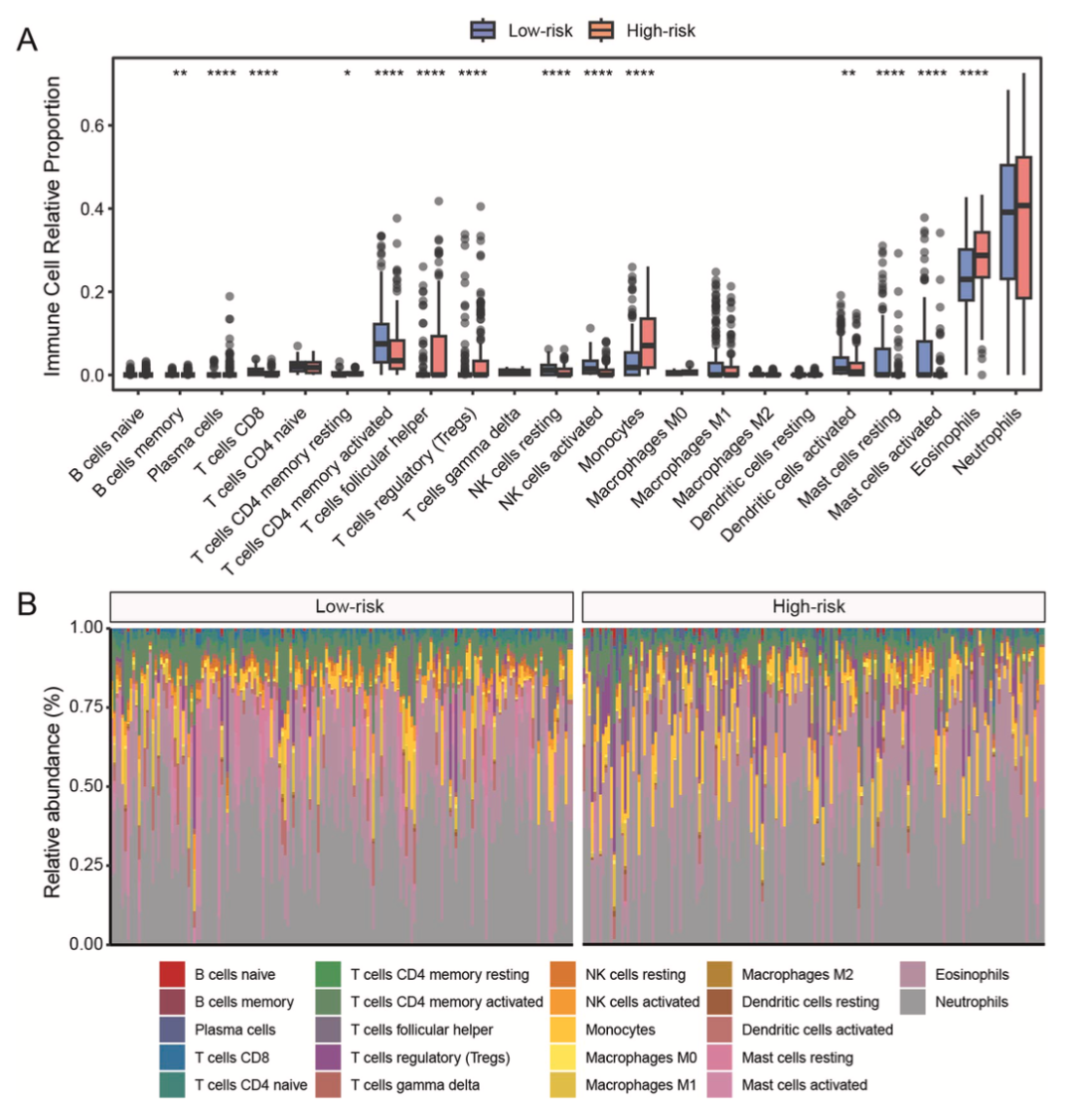
免疫微环境分析
比较两组之间免疫细胞浸润的差异(图4A),其中的14种免疫细胞类型之间存在显著差异。低风险组表现出更高的抗肿瘤免疫细胞浸润(图4B)。因为低风险患者表现出更丰富的抗肿瘤作用的免疫细胞浸润,因此可以认为低风险患者的OS更高。
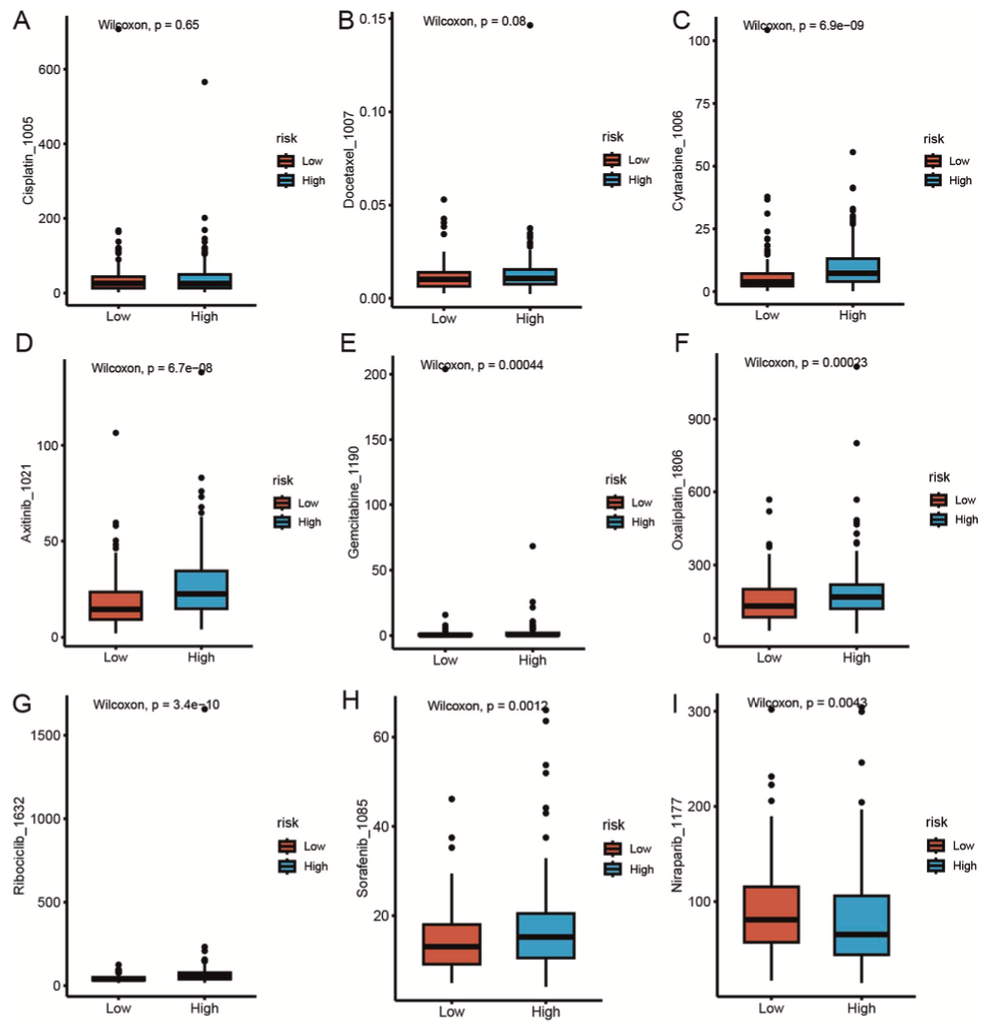
药物敏感性分析
使用Wilcoxon检验来体现两个风险组之间对常用药物的敏感性差异,对于低风险组来说,其对阿昔替尼、阿糖胞甘、吉西他滨、奥沙利铂、sorafenib和瑞博西尼等药物的敏感性更高(图5A-I)。根据以上的分析结果提出了可以利用不同药物的敏感性差异,根据风险分层制定个性化的治疗策略从而提高治疗效果和患者预后的潜力这一结论。
文章小结
现在相信你对整个文章的思路已经有了自己的认识,小云再带大家总结一下:这篇文章从数据获取与处理着手,之后构建了4个风险模型并进行验证,随后根据基因表达数据、临床信息和肿瘤免疫微环境特征,构建了具有临床应用前景的预后和药物敏感性模型,最后对胃癌的预后和治疗提供了新的想法。这篇文章强就强在逻辑完整清晰,我们之后在发文时思路一定要理清,工欲善其事,必先利其器,有了一个清晰的思路是一篇好文的前提,“0实验”轻轻松松就能发中科院2区。复现有困难的宝子们,来找豆豆就对啦~你想做的,豆豆都能帮助你,心动不如手动!